Лікарські засоби є ключовим інструментом сучасної медицини, проте їх ефективність визначається не лише хімічною структурою, а й складним шляхом, який вони проходять в організмі. Від моменту прийому таблетки до взаємодії з клітинними структурами відбувається низка процесів — розчинення, абсорбція, метаболізм, розподіл і, зрештою, фармакодинамічна дія. Розуміння цього шляху має фундаментальне значення як для фахівців, так і для пацієнтів.
«Правило п’яти», сформульоване Крістофером Ліпінським у 1997 році, окреслило ключові параметри вибору активних фармацевтичних інгредієнтів.
Правило п’яти зазвичай допомагає передбачити, чи будуть таблетки добре всмоктуватися в шлунку та кишечнику. Але є речовини, які зневажають на ці правила — це протигрибкові засоби, вітаміни, серцеві глікозиди. Ці молекули занадто великі, занадто важкі або занадто складні, щоб просто «просочитися» крізь стінки клітин. Але вони все одно ефективні. Секрет у тому, що вони не чекають, поки їх впустять — вони «зламують» систему транспортування.

Серцеві глікозиди (наприклад, дигоксин) мають специфічну структуру (стероїдне ядро + цукри). Організм сприймає їх як «своїх» і використовує спеціальні білки-переносники, щоб затягнути їх всередину клітини. Вони їдуть на «таксі», замість того, щоб іти пішки крізь мембрану.
Більшість вітамінів — це великі та складні молекули. Якби вони покладалися лише на пасивне всмоктування, ми б страждали від їх дефіциту. Еволюція створила для них активні транспортні системи. Наприклад, вітамін В12 зв’язується зі спеціальним білком (фактором Касла), який буквально за руку проводить його в кров.
Протигрибкові засоби (наприклад, амфотерицин В) часто мають величезні молекули, які ніяк не вписуються в ліміти ваги (500 Дальтон). Проте вони мають унікальну здатність вбудовуватися в мембрани грибків, імітуючи їхні природні компоненти (ергостерол). Вони діють як «троянський кінь».
Подальші дослідження показали, що швидкість розчинення та стабільність у шлунково-кишковому тракті є критичними факторами для ефективності таблетованих форм і залежать від властивостей АФІ і допоміжних речовин.
Фармацевтичні лікарські форми складаються з активних фармацевтичних інгредієнтів (АФІ) та допоміжних речовин. Допоміжні речовини покращують технологічність виробництва, забезпечують стабільність і підвищують прийнятність препарату для пацієнтів. Вони можуть виступати в ролі носіїв, стабілізаторів, солюбілізаторів або модуляторів вивільнення лікарської речовини. Дедалі більше досліджень підкреслюють їхній прямий вплив на безпеку, ефективність та якість продукту. Допоміжні речовини контролюють вивільнення лікарського засобу, впливаючи на процеси розчинення та дифузії.
У таблетках негайного вивільнення ключову роль відіграють:
- Розпушувачі (дезінтегранти), які при контакті з вологою швидко вбирають воду і набрякають, створюючи внутрішній тиск, який буквально «підриває» таблетку зсередини.
- Наповнювачі та зв’язуючі речовини, які, не перешкоджаючи змочуванню та швидкому розчиненню частинок препарату, формують якісну таблетку.
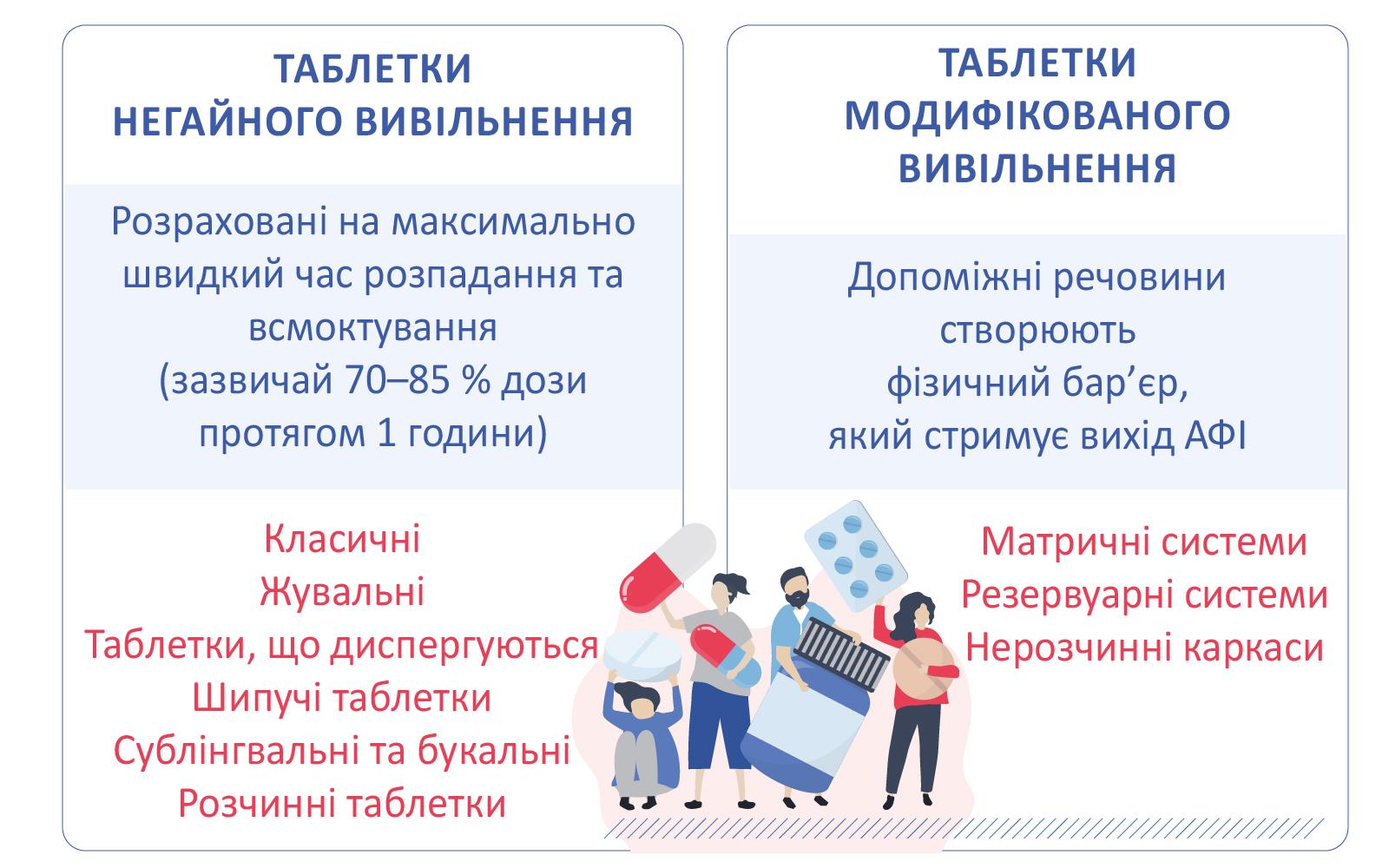
Таблетки модифікованого вивільнення залежно від утвореного типу здатні змінювати вивільнення АФІ. Таблетки з матричною системою рівномірно розподіляють АФІ в сітці з полімерів (наприклад, ГПМЦ — гідроксипропілметилцелюлоза). При потраплянні в середовище полімер набрякає і створює щільний гідрогелевий шар. Діюча речовина повільно просочується крізь цей гель (дифузія) або вивільняється в міру поступового розмивання самого гелю (ерозія).
У таблетованих формах з резервуарною системою ядро покривається спеціальною полімерною плівкою, яка не розчиняється відразу. АФІ виходять назовні лише крізь мікроскопічні пори в цій оболонці з постійною швидкістю.
У таблетках з нерозчинним каркасом використовуються речовини (воски), які не перетравлюються. АФІ просто «вимиваються» з цього каркаса, а сама порожня матриця згодом виводиться з організму.
Отже, у системах негайного типу допоміжні речовини руйнують структуру таблетки для збільшення площі контакту з рідиною, а в уповільнених — утримують її, регулюючи швидкість руху молекул АФІ у зовнішнє середовище. Саме допоміжні речовини визначають тривалість терапевтичного ефекту та можуть підвищити біодоступність.
Коли таблетка потрапляє до рота, її доля залежить від того, на який сценарій її «запрограмували» технологи. Що відбувається з різними типами таблеток, можна побачити у таблиці 1.
Таблиця 1
Що відчуває таблетка і ваш організм — після проковтування
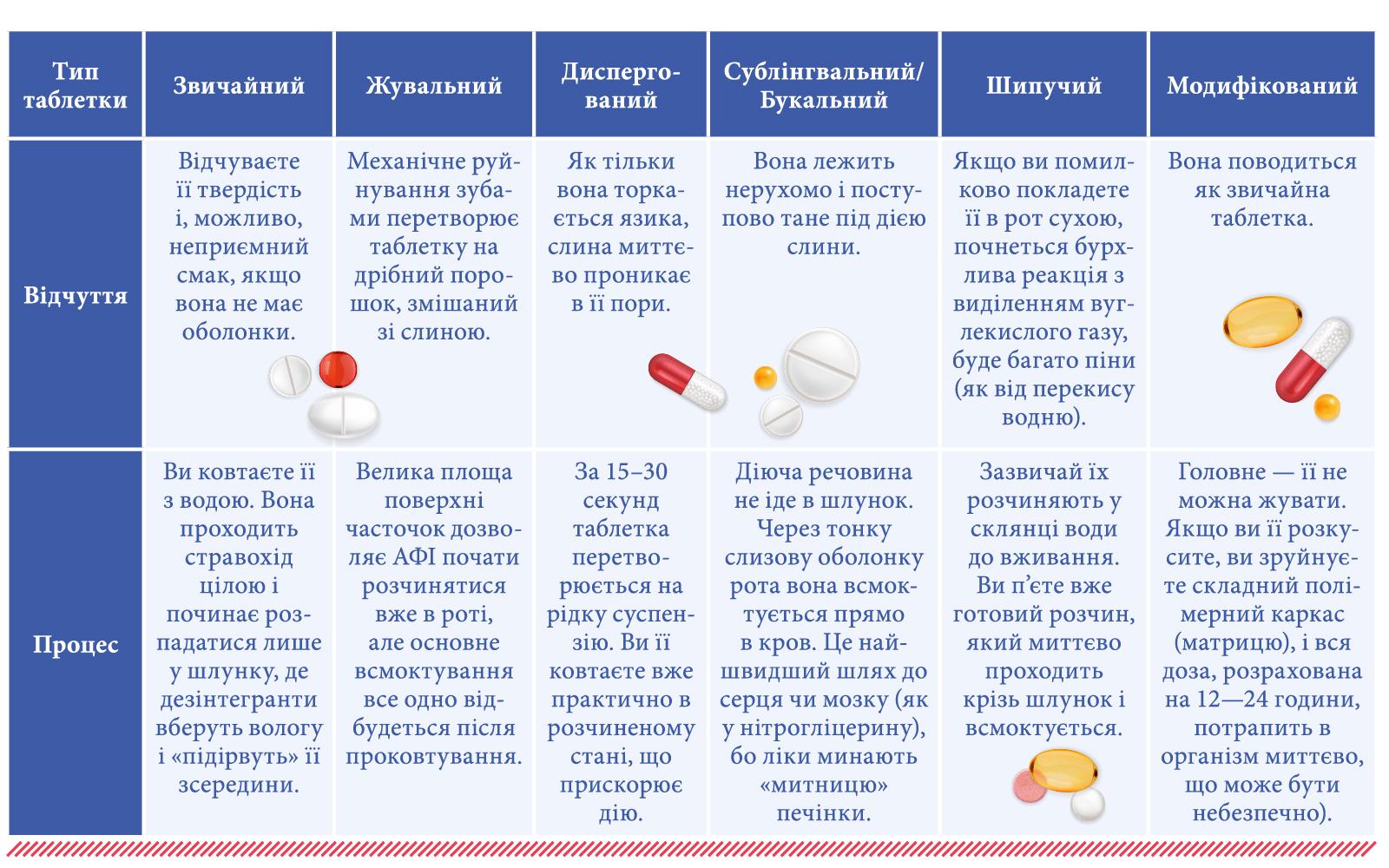
Тобто, ротова порожнина для таблетки — це або просто «транзитний коридор» (для звичайних), або «активний майданчик» для миттєвого розпаду чи прямого всмоктування (для спеціальних форм).
Після того, як таблетка залишає ротову порожнину, її шлях у шлунково-кишковому тракті (ШКТ) нагадує проходження через різні хімічні цехи. Ось що з ними стається (табл. 2).
Таблиця 2
Фармакокінетика на дотик: як різні таблетки взаємодіють з організмом

Щоб краще зрозуміти, чому різні таблетки діють по-різному, варто подивитися на їхню «фармакокінетичну поведінку». Одні створені для швидкого ефекту, інші — для тривалого й контрольованого вивільнення. На рисунку показано, як саме тип таблетки впливає на швидкість початку дії та її тривалість.
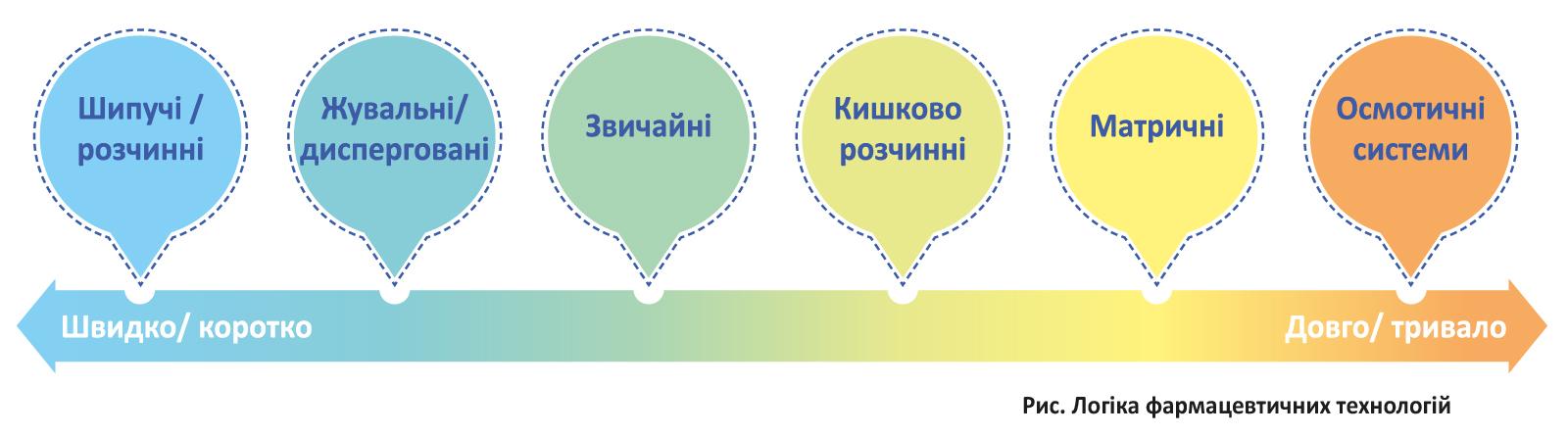
Рисунок наочно демонструє логіку фармацевтичних технологій: від швидких, але короткочасних форм (шипучі, жувальні, дисперговані) до складних систем із контрольованим вивільненням (матричні та осмотичні). Це дозволяє лікарям і фармацевтам підбирати оптимальну форму залежно від потреб пацієнта - чи потрібен миттєвий ефект, чи стабільна дія протягом доби.
Коли ліки розчинилися, вони мають пройти крізь стінку кишечника за рахунок пасивної дифузії та активного транспорта. Саме тут АФІ, якщо відповідає правилу Ліпінського, проходитиме крізь мембрану або білки-переносники хапають молекулу і затягують її всередину (як у випадку з вітамінами). Хоча більшість АФІ всмоктується в тонкому кишечнику, процес може починатися ще в шлунку (для деяких кислот), хоча кишечник - це основна «магістраль» завдяки величезній площі поверхні.
Саме допоміжні речовини (наприклад, певні жирні кислоти або хелатори) можуть тимчасово «розхитувати» щільні контакти між клітинами кишечника, щоб ліки пройшли швидше. Інші допоміжні речовини (наприклад, деякі неіонні ПАР, як-от водорозчинна похідна натурального вітаміну Е або поліетиленгліколі) можуть блокувати білки-відкачувачі (P-глікопротеїн), які намагаються викинути ліки назад у кишечник.
Коли ми приймаємо ліки, вони потрапляють у печінку, де працює ціла армія ферментів. Найвідоміші з них — цитохроми P450. Їхня робота нагадує митників: вони перевіряють молекулу і «прикріплюють» до неї атом кисню або змінюють її структуру так, щоб вона стала більш полярною. А оскільки наша кров і сеча — водні середовища, така молекула легше циркулює і швидше виводиться через нирки. Це перший етап біотрансформації: організм перетворює «чужорідні» молекули на більш безпечні та придатні для виведення. Як приклад можна привести знайомі всім препарати. Нітрогліцерин швидко метаболізується у печінці, тому його часто дають під язик — щоб оминути «митницю» і діяти миттєво. Парацетамол у нормальних дозах окиснюється без проблем, але при передозуванні утворюються токсичні метаболіти, які можуть пошкодити печінку. Отже, можна сказати, що ферменти P450 — це «хімічні майстри», які роблять молекули більш гідрофільними, щоб організм міг їх легко позбутися.
Після того як ферменти цитохрому P450 зробили молекулу більш полярною (Фаза I), організм переходить до наступного кроку — кон’югації. Це ніби «прикріплення хвостика» до молекули. Найчастіше таким хвостиком є глюкуронова кислота, але можуть бути й інші — сульфат, ацетат, гліцин. Цей хвостик робить її не просто розчинною, а й електрично зарядженою. Це фінальний етап «хімічної митниці» — після нього молекула вже не становить загрози й залишає організм.
Саме на етапі першого проходження ліків крізь стінку кишечника та печінку деякі ексципієнти (наприклад, певні олії або ПАР) можуть тимчасово «відволікати» або сповільнювати ферменти (такі як CYP3A4). Це не дає ферментам передчасно зруйнувати молекулу, дозволяючи більшій частині ліків у незміненому вигляді дійти до цілі. Таким чином, вони допомагають подолати ефект першого проходження і суттєво підвищують біодоступність.
Після цього АФІ потрапляють у кров і мають дістатися до потрібного органу або шляхом зв’язування з білками, або таргетування. Більшість АФІ «прилипають» до альбуміну крові, який є тимчасовим «депо». Тільки «вільні» молекули (не зв’язані з білком) можуть вийти з крові в тканини та діяти. Допоміжні речовини тут грають непряму роль: вони забезпечують таку швидкість вивільнення з таблетки, щоб білки крові не «зв’язали» все одразу, залишаючи частину молекул для негайної дії. При таргетуванні допоміжні речовини працюють як адресна доставка. Вони ховають АФІ від імунної системи та білків плазми, доставляючи їх прямо до пухлини чи осередка запалення.
***
ВАЖЛИВО!
При передозуванні система кон’югації перевантажується, і утворюються токсичні метаболіти (через альтернативний шлях окиснення). Вони можуть пошкодити печінку — тому парацетамол часто наводять як класичний приклад балансу між безпечним метаболізмом і ризиком.
***
Фінальна точка — зустріч молекули з рецептором на поверхні або всередині клітини. Лікарські препарати працюють як «ключ до замка». Вони або запускають процес (агоністи), або блокують його (антагоністи). На цьому етапі допоміжні речовини вже зазвичай відсутні, але саме вони забезпечили доставку потрібної концентрації молекул АФІ до рецептора в потрібний момент. Без правильних допоміжних речовин ліки могли б просто не дістатися до «замка» або зруйнуватися по дорозі.
Отже, допоміжні речовини — це не просто «пасивний наповнювач» лікарських засобів, це інтелектуальна система логістики та безпеки АФІ. Вони забезпечують проходження через «митницю» (кишечник), захищають від «утилізації» (печінка) і допомагають «адресній доставці» до клітин-мішеней. Без цієї інфраструктури навіть найпотужніша молекула АФІ була б безпорадною, оскільки вона або не розчинилася б, або була б знищена організмом ще до того, як знайде свою ціль.
Таким чином, шлях від таблетки до клітини — це не просто пасивне переміщення, а високотехнологічний процес керування біодоступністю. Сучасна фармацевтика навчилася обходити природні бар’єри (як у випадку з винятками правила Ліпінського) та програмувати поведінку молекул за допомогою допоміжних речовин. Це перетворює звичайну таблетку на складну інтелектуальну систему доставки, де кожен компонент працює на точність та безпеку терапії.
Інна Ковалевська, доктор фармацевтичних наук, професор НФаУ
Список літератури знаходиться в редакції.










