Ганна Кирпач, лікар загальної практики
Осінь підкрадається непомітно, але разом з нею приходить і нова хвиля занепокоєння — епідемія COVID-19 не відступила. Так, у період із 25 до 31 серпня 2025 року в Україні було зареєстровано 10 622 нові випадки COVID-19, що на 46,2 % більше, ніж тижнем раніше [1]. Ці цифри — не просто статистика. Вони свідчать, що епідемія знову посилюється саме тоді, коли сезон респіраторних інфекцій лише набирає обертів. Очікується, що пік може припасти на жовтень-листопад. У цей період особливо важливо своєчасно вживати заходів, адже медична інфраструктура ще здатна витримати додаткове навантаження, а наявні захисні стратегії зберігають ефективність. Противірусна терапія розглядається як один із ключових інструментів, що може знизити ризик розвитку хронічних ускладнень, зменшити кількість госпіталізацій та запобігти критичному тиску на систему охорони здоров’я.
Коли варто запідозрити COVID-19?
COVID-19 може проявлятися по-різному — від легких симптомів до тяжких ускладнень. Важливо вчасно звернути увагу на перші ознаки, щоб не згаяти дорогоцінний час і почати лікування якомога раніше.
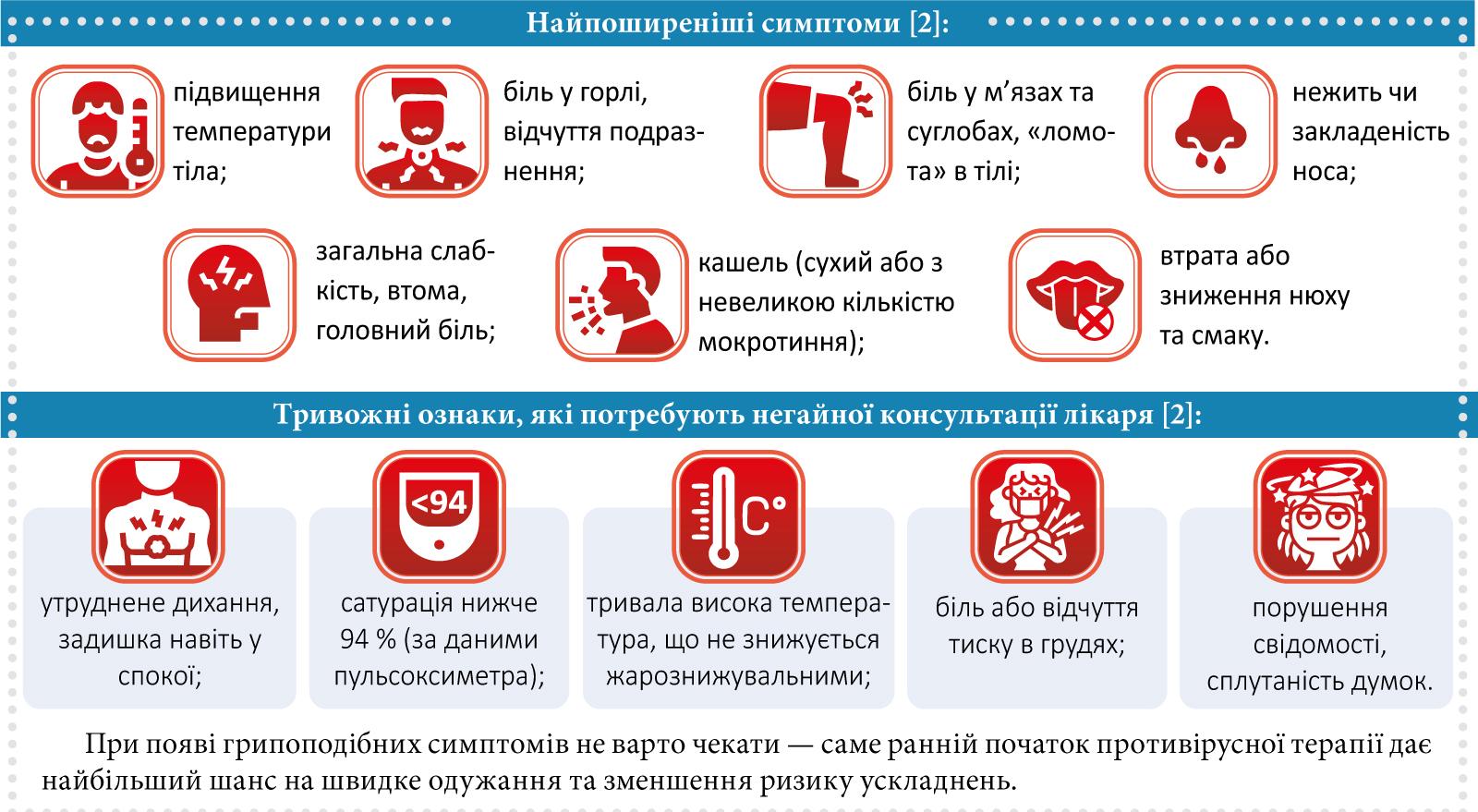
При появі грипоподібних симптомів не варто чекати — саме ранній початок противірусної терапії дає найбільший шанс на швидке одужання та зменшення ризику ускладнень.
Як діагностувати COVID-19?
Для підтвердження діагнозу COVID-19 сьогодні доступні як швидкі експрес-тести, так і лабораторні методи.
Експрес-тести (швидка діагностика) [3]: доступні в аптеках і можуть виконуватися самостійно вдома. Вони ґрунтуються на виявленні антигенів SARS-CoV-2 у мазку з носоглотки та дозволяють отримати результат уже через 15–20 хвилин. Найбільш інформативними такі тести є у перші дні захворювання, коли вірусне навантаження найвище. Їх використовують для попередньої діагностики, однак у випадку негативного результату за наявності симптомів рекомендується підтвердити діагноз лабораторними методами.
Лабораторні дослідження [3]:
- ПЛР-тест (полімеразна ланцюгова реакція) — «золотий стандарт» діагностики COVID-19. Виявляє вірусну РНК у мазку з носоглотки. Має високу чутливість і специфічність.
- Тести на антиген у лабораторії — швидший і дешевший метод, який виявляє вірусні антигени; дещо менш чутливий, ніж ПЛР.
- Серологічні тести (IgM/IgG до SARS-CoV-2) — визначають наявність антитіл у крові, що свідчить про перенесену інфекцію або імунну відповідь після вакцинації. Використовуються не для гострої діагностики, а для оцінки імунного статусу.
Таким чином, експрес-тести дозволяють швидко зорієнтуватися, але остаточне підтвердження діагнозу забезпечують лабораторні методи, насамперед, ПЛР.
Небезпеки нелікованого COVID-19
COVID-19 — це не лише гостра респіраторна інфекція. У значної частини пацієнтів після перенесеної хвороби розвиваються проблеми, що виходять далеко за межі дихальної системи. Ці наслідки можуть зберігатися місяцями або навіть роками, істотно знижуючи якість життя та підвищуючи ризик передчасної смерті. Найбільш вивчені та клінічно значущі ускладнення стосуються серцево-судинної системи, головного мозку, коагуляційного гомеостазу та когнітивних функцій.
Серцево-судинні порушення
COVID-19 може залишати довготривалий слід у роботі серцево-судинної системи. Навіть через рік після інфекції у людей частіше діагностують аритмії, серцеву недостатність, ішемічну хворобу серця та міокардит. Ризик цих проблем зростає навіть у тих, хто хворів відносно легко [4].
Ризик інсульту також помітно зростає. За даними шведського дослідження, у перший тиждень після інфекції ймовірність інсульту чи інфаркту може бути у 3–8 разів вищою, ніж у людей, які не хворіли на COVID-19 [5].
Постковідні когнітивні розлади та деменція
Все більше наукових праць свідчать, що COVID-19 здатний прискорювати вікові зміни мозку. У літніх пацієнтів після хвороби зростає ризик розвитку нової деменції. У частини людей навіть після легкого перебігу спостерігають проблеми з пам’яттю, увагою та мисленням, які нагадують ранні прояви когнітивного дефіциту [7, 8].
Тромбози
COVID-19 порушує систему згортання крові, створюючи схильність до тромбоутворення. Навіть через кілька місяців після гострої інфекції ризик легеневої емболії чи глибокого венозного тромбозу лишається підвищеним.
Так, у роботі Katsoularis було встановлено, що [9]:
- ризик легеневої емболії у перші 30 днів після COVID-19 зростав у 33 рази;
- ризик глибокого венозного тромбозу — у 5 разів;
- підвищений ризик зберігався до 6 місяців після інфекції.
Такі наслідки підкреслюють: боротьба з COVID-19 не може зводитися лише до симптоматичного лікування. Своєчасне призначення адекватної терапії, зокрема, противірусних препаратів, є ключовим для зменшення ризику тяжких подій та захисту пацієнтів у довгостроковій перспективі. Серед сучасних противірусних засобів особливе місце посідає фавіпіравір — молекула з доведеною активністю проти РНК-вірусів, включно з SARS-CoV-2. В Україні єдиним препаратом на його основі є Ковіфлу, що внесений до національного Протоколу надання медичної допомоги при COVID-19.

Як діє фавіпіравір?
Фавіпіравір належить до групи противірусних засобів, що пригнічують реплікацію РНК-вірусів. Його механізм дії ґрунтується на інгібуванні ферменту РНК-залежної РНК-полімерази (RdRp) — ключового ензиму, який відповідає за копіювання вірусного геному.
Після потрапляння в організм фавіпіравір метаболізується до активної форми — фавіпіравір-рибозо-трифосфату. Цей метаболіт вбудовується в ланцюг вірусної РНК замість природних нуклеотидів. У результаті виникають помилки у синтезі, які блокують подальше копіювання геному й перешкоджають формуванню повноцінних віріонів. Таким чином, вірус втрачає здатність до розмноження й поширення в організмі [10].
Особливість препарату полягає у широкому спектрі активності проти різних РНК-вірусів, включно з грипом, вірусами геморагічних лихоманок та коронавірусами. Дослідження in vitro показали ефективне пригнічення реплікації SARS-CoV-2, що стало підставою для клінічного застосування при COVID-19 [11].

Фавіпіравір: що говорять результати досліджень
Ефективність і безпека фавіпіравіру при лікуванні COVID-19 підтверджені низкою клінічних досліджень у різних країнах світу. Вони охоплювали як госпіталізованих пацієнтів із помірним перебігом пневмонії, так і амбулаторних хворих із легким або середнім ступенем тяжкості. У більшості досліджень застосування препарату асоціювалося зі швидшим зникненням симптомів, скороченням тривалості гарячки та госпіталізації, а також із більш швидким.
Так, Cai та співавтори провели відкрите проспективне контрольоване дослідження за участю пацієнтів із підтвердженим COVID-19 [15]. Група фавіпіравіру (n=35) отримувала препарат у стандартному дозуванні (1600 мг двічі на добу в 1-й день, далі 600 мг двічі на добу до 14 днів) у поєднанні з інгаляціями інтерферону (IFN)-α, а контрольна група (n=45) — лопінавір/ритонавір + IFN-α. Первинно оцінювали час до повної елімінації вірусу та динаміку змін на КТ. Уже на 4-й день у групі фавіпіравіру відзначалося достовірно швидше зникнення вірусної РНК (медіана 4 дні проти 11 днів у контролі; p<0,001). Крім того, рентгенологічне покращення на КТ спостерігалося у 91,4 % пацієнтів, що було значно вище, ніж у контрольній групі (62,2 %; p=0,004). Небажані явища траплялися рідше у групі фавіпіравіру.

У ще одному рандомізованому багатоцентровому дослідженні (фаза III) взяли участь 150 амбулаторних пацієнтів із легким та середньотяжким COVID-19 [16]. Учасників у співвідношенні 1:1 розподілили на групу, яка отримувала стандартну терапію з додаванням фавіпіравіру (1800 мг двічі на добу в 1-й день, далі 800 мг двічі на добу до 14 днів), та контрольну групу лише на стандартному лікуванні. Первинною кінцевою точкою був час до припинення виділення вірусу; також вимірювали час до клінічного одужання. В результаті було встановлено, що час до клінічного одужання скоротився: 3 дні у групі фавіпіравіру проти 5 днів у контролі (p=0,030). Також відзначалися швидша нормалізація температури та сатурації.
У Японії було проведено рандомізоване плацебо-контрольоване дослідження (РКД) фази III серед госпіталізованих хворих із помірною пневмонією без потреби у кисневій підтримці (n=156) [17]. Первинна кінцева точка була композитною і включила час до нормалізації температури, сатурації периферичної крові киснем (SpO₂), рентгенологічного поліпшення та негативізації ПЛР. Фавіпіравір скоротив медіану часу до досягнення композитної точки: 11,9 дня проти 14,7 дня у плацебо (p=0,0136). Ефект був виразнішим за раннього початку лікування та за наявності факторів ризику; летальних випадків не зафіксовано.
Також у Таїланді проведено багатоцентрове рандомізоване відкрите дослідження в пацієнтів із раннім COVID-19 без пневмонії (n=93) [18]. Фавіпіравір застосовували у дозуванні 1800 мг двічі на добу в 1-й день, далі 800 мг двічі на добу 5–14 днів. Первинною кінцевою точкою був час до настання стійкого клінічного поліпшення за шкалою NEWS≤1. В результаті було встановлено, що у групі фавіпіравіру медіана часу до стійкого клінічного покращення за шкалою NEWS становила лише 2 дні проти 14 днів у контрольній групі (p<0,001). Автори підкреслили, що ранній початок терапії дозволяє досягати значно швидшої динаміки.
На базі кількох клінічних центрів було проведено відкрите рандомізоване дослідження з метою оцінки ефективності та безпеки фавіпіравіру у лікуванні COVID-19 [19]. Усього до нього включили 96 дорослих пацієнтів із підтвердженою інфекцією SARS-CoV-2.
Пацієнтів розподілили на дві групи:
- основна група (n≈48) отримувала фавіпіравір у дозуванні 1600 мг двічі на добу в 1-й день, далі по 600 мг двічі на добу протягом до 14 днів;
- контрольна група (n≈48) отримувала терапію хлорохіном у стандартних дозах.
Первинними кінцевими точками були потреба в штучній вентиляції легень (ШВЛ) та летальність. Додатково оцінювали тривалість госпіталізації, клінічне покращення та безпеку терапії.
В результаті жоден із пацієнтів, які приймали фавіпіравір, не потребував переведення на апарат ШВЛ, тоді як у контрольній групі такі випадки все ж зафіксували. Летальність у групі фавіпіравіру становила лише 2,3 % проти 4,2 % у пацієнтів, які отримували хлорохін. Крім того, у групі фавіпіравіру спостерігалося скорочення тривалості госпіталізації: пацієнти швидше виписувалися додому, відновлюючи працездатність. Побічні реакції були поодинокими та не перевищували очікуваний профіль безпеки: переважно спостерігалося транзиторне підвищення рівня сечової кислоти та легкі шлунково-кишкові розлади. Жодних серйозних ускладнень терапії не зареєстрували. У підсумку автори зробили висновок, що фавіпіравір не лише сприяє швидшій клінічній динаміці, а й має потенціал зменшувати навантаження на систему охорони здоров’я у періоди епідемічних хвиль.
Таким чином, фавіпіравір підтвердив свою клінічну значущість у боротьбі з COVID-19, поєднуючи ефективність і сприятливий профіль безпеки.
Переваги Ковіфлу
Включення до національного Протоколу лікування COVID-19
Ковіфлу є офіційно затвердженим препаратом для застосування при SARS-CoV-2 в Україні, що підтверджує його значущість та довіру з боку системи охорони здоров’я.
Доведена противірусна активність
Ковіфлу безпосередньо блокує розмноження SARS-CoV-2, зменшуючи вірусне навантаження та запобігаючи прогресуванню інфекції. Крім того, він проявляє активність проти вірусу грипу, що особливо важливо у сезоні циркуляції кількох респіраторних патогенів.
Швидше клінічне одужання
Прийом Ковіфлу дозволяє скоротити час до зникнення основних симптомів (лихоманки, кашлю, задишки), нормалізації сатурації та рентгенологічного покращення. Це означає швидше повернення до активного життя.
Зменшення ризику госпіталізації та ускладнень
Клінічні дані свідчать, що пацієнти, які отримували фавіпіравір, рідше потребували кисневої терапії чи переведення на ШВЛ. Це робить Ковіфлу важливим інструментом для зниження навантаження на систему охорони здоров’я.
Оптимальний профіль безпеки
Побічні ефекти Ковіфлу зазвичай є легкими та минущими (тимчасове підвищення рівня сечової кислоти, легкі шлунково-кишкові розлади) і не потребують відміни терапії. Жодних серйозних ускладнень не зафіксовано.
Зручність застосування
Ковіфлу доступний у формі таблеток для перорального прийому, що дозволяє проводити лікування як у стаціонарі, так і в амбулаторних умовах.
Виробництво за стандартами GMP
Ковіфлу виготовляється на виробничих потужностях, що відповідають міжнародним вимогам належної виробничої практики (GMP). Це гарантує високу якість, безпечність та стабільність кожної серії препарату, що є особливо важливим для терапії інфекційних захворювань.
Як приймати Ковіфлу?
Застосування препарату слід розпочати негайно після появи перших грипоподібних симптомів (підвищення температури, кашель, біль у горлі, ломота в тілі тощо). Ранній початок терапії є ключовим фактором ефективності лікування.
Загальний період терапії становить 5 днів.
- 1-й день лікування — по 1600 мг (8 таблеток) двічі на добу.
- 2–5-й дні — по 600 мг (3 таблетки) двічі на добу.
Таблетки слід приймати перорально, запиваючи достатньою кількістю води, незалежно від прийому їжі.

Висновок
COVID-19 і надалі залишається серйозним викликом для системи охорони здоров’я та суспільства. Дані клінічних досліджень свідчать, що фавіпіравір має доведену ефективність у зниженні вірусного навантаження, скороченні тривалості симптомів та зменшенні ризику ускладнень. В Україні єдиним препаратом на його основі є Ковіфлу — противірусний засіб із доведеним механізмом дії, зручним пероральним прийомом, хорошим профілем безпеки та виробництвом відповідно до міжнародних стандартів GMP.
Своєчасне застосування Ковіфлу дозволяє не лише покращити перебіг захворювання у конкретного пацієнта, але й зменшити тиск на систему охорони здоров’я під час епідемічних хвиль. Це робить препарат важливим інструментом у комплексній стратегії боротьби з COVID-19 та сезонними респіраторними інфекціями.
Список використаної літератури:
- Public Health Center of the Ministry of Health of Ukraine. Weekly COVID-19 report, 25–31 August 2025; cited in PRM News, “COVID-19 cases are growing in Ukraine,” 2 September 2025
- Centers for Disease Control and Prevention. Symptoms of COVID-19. CDC, 2024. Available from: https://www.cdc.gov/covid/signs-symptoms/index.html
- World Health Organization. Diagnostic testing for SARS-CoV-2: interim guidance. WHO, 2020. Available from: https://www.who.int/publications/i/item/diagnostic-testing-for-sars-cov-2
- Xie Y, Bowe B, Al-Aly Z. Long-term cardiovascular outcomes of COVID-19. Nature Medicine. 2022 Mar;28(3):583–590. doi:10.1038/s41591-022-01689-3. PMID: 35132265.
- Katsoularis I, Fonseca-Rodríguez O, Farrington P, Lindmark K, Fors Connolly AM. Risk of acute myocardial infarction and ischaemic stroke following COVID-19 in Sweden: a self-controlled case series and matched cohort study. Lancet. 2021 Aug 14;398(10300):599–607. doi: 10.1016/S0140-6736(21)00896-5.
- Bruno RM, Badhwar S, Abid L, et al.; the CARTESIAN Investigators. Accelerated vascular ageing after COVID-19 infection: the CARTESIAN study. European Heart Journal. 2025 Aug 17:eha f430. doi:10.1093/eurheartj/ehaf430
- Shan D, Wang C, Crawford T, Holland C. Association between COVID-19 infection and new-onset dementia in older adults: a systematic review and meta-analysis. BMC Geriatrics. 2024 Dec 15; 24(1): 940. doi: 10.1186/s12877-024-05538-5
- Doskas T. Neurocognitive Impairment After COVID-19: Mechanisms, Phenotypes, and Links to Alzheimer’s Disease. Brain Sciences. 2025; 15(6): 564
- Katsoularis I, Fonseca-Rodriguez O, Farrington P, Lindmark K, Fors Connolly AM. Risk of deep vein thrombosis, pulmonary embolism, and bleeding after COVID-19: nationwide self-controlled case series and matched cohort study. BMJ. 2022 Apr 6;377:e069590. doi:10.1136/bmj-2021-069590. PMID: 35387772; PMCID: PMC8979876.
- Furuta Y, Komeno T, Nakamura T. Favipiravir (T-705), a broad spectrum inhibitor of viral RNA polymerase. Proc Jpn Acad Ser B Phys Biol Sci. 2017;93(7):449-463. doi:10.2183/pjab.93.027
- Shiraki K, Daikoku T. Favipiravir, an anti-influenza drug against life-threatening RNA virus infections. Pharmacol Ther. 2020;209:107512. doi:10.1016/j.pharmthera.2020.107512
- Golpour M, Jalali H, Alizadeh-Navaei R, Rezaei Talarposhti M, Mousavi T, Nadi Ghara AA, et al. Co-infection of SARS-CoV-2 and influenza A/B among patients with COVID-19: a systematic review and meta-analysis. BMC Infect Dis. 2025;25:940. doi:10.1186/s12879-025-10521-5
- Adams K, Tastad K, Huang S. Prevalence of SARS-CoV-2 and Influenza Coinfection and Clinical Characteristics Among Children and Adolescents Aged <18 Years Who Were Hospitalized or Died with Influenza — United States, 2021-22 Influenza Season. MMWR Morb Mortal Wkly Rep. 2022;71(50):1589-1596. doi:10.15585/mmwr.mm7150a4
- Joshi S, Parkar J, Ansari A, Vora A, Talwar D, Tiwaskar M, Patil S, Barkate H. Role of favipiravir in the treatment of COVID-19. Int J Infect Dis. 2021 Mar;102:501-508. doi:10.1016/j.ijid.2020.10.069
- Cai Q, Yang M, Liu D, Chen J, Shu D, Xia J, et al. Engineering (Beijing). 2020;6(10):1192–1198. doi:10.1016/j.eng.2020.03.007
- Udwadia ZF, Singh P, Barkate H, Patil S, Rangwala S, Pendse A, Kadam J, Wu W, Caracta CF, Tandon M. Efficacy and safety of favipiravir, an oral RNA-dependent RNA polymerase inhibitor, in mild-to-moderate COVID-19: A randomized, comparative, open-label, multicenter, phase 3 clinical trial. Int J Infect Dis. 2021 Feb;103:62-71. doi: 10.1016/j.ijid.2020.11.142.
- Shinkai M, Tsushima K, Tanaka S, Hagiwara E, Tarumoto N, Kawada I, et al. Efficacy and Safety of Favipiravir in Moderate COVID-19 Pneumonia Patients without Oxygen Therapy: A Randomized, Phase III Clinical Trial. Infectious Diseases and Therapy. 2021;10(4):2489–2509. doi:10.1007/s40121-021-00517-4
- Sirijatuphat R, Manosuthi W, Niyomnaitham S, Owen A, Copeland KK, Charoenpong L, et al. Early treatment of Favipiravir in COVID-19 patients without pneumonia: a multicentre, open-labelled, randomized control study. Emerging Microbes & Infections. 2022;11(1):2197–2206. doi:10.1080/22221751.2022.2117092
- Dabbous HM, Abd-Elsalam S, El-Sayed MH, Sherief AF, Ebeid FFS, El Ghafar MSA, Soliman S, Elbahnasawy M, Badawi R, Tageldin MA. Efficacy of favipiravir in COVID-19 treatment: a multicenter randomized study. Arch Virol. 2021;166(3):949–954. doi:10.1007/s00705-021-04956-9