Объекты исследования
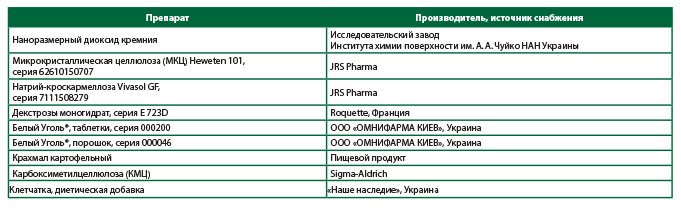
В качестве объектов исследования были выбраны следующие препараты (Табл. 1).Таблица 1. Объекты исследования
ИК-спектроскопическое исследование
ИК-спектры снимали с помощью прибора Specord М-80 (Carl Zeiss, Германия). Препараты смешивали с калия бромидом 1:100 и прессовали в виде таблеток, которые подвергали анализу в диапазоне 4000–400 см-1. Результаты приведены на рис. 1–5.Все ИК-спектры, кроме спектра диоксида кремния, являются подобными, что свидетельствует о том, что исследуемые вещества относятся к одному химическому классу — высокомолекулярным производным глюкозы.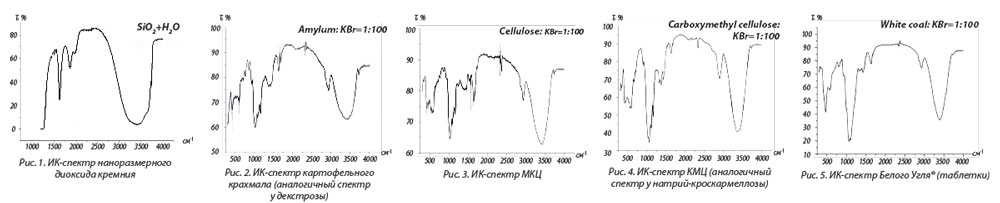

Адсорбция метиленового синего
В качестве тест-вещества для изучения адсорбции положительно заряженных низкомолекулярных соединений (алкалоиды, гистамин, димедрол, новокаина гидрохлорид, промедол и т. п.) используют катионный краситель метиленовый синий (М.м. = 320 г/моль).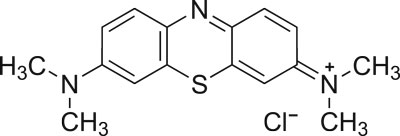
Рис. 6. Метиленовый синий
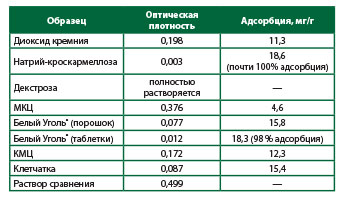
Методика испытанияИсследуемый раствор. К 0,08 г (точная навеска) сорбента добавляют 10 мл 0,15 мг/мл раствора метиленового синего, встряхивают на аппарате для встряхивания на протяжении 1 часа, потом центрифугируют при частоте вращения 6000 оборотов в минуту на протяжении 20 минут. 1 мл надосадочной жидкости доводят водой до 50 мл.Раствор сравнения. 1 мл 0,15 мг/мл раствора метиленового синего доводят водой до 50 мл.Измеряют оптическую плотность исследуемого раствора и раствора сравнения при длине волны 670 нм в кювете толщиной 2 см. В качестве компенсационного раствора используют воду.Адсорбционную активность препарата (Х, мг/г) рассчитывают по формуле: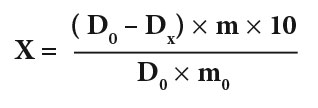
Таблица 2. Результаты измерений
- 80 мг × 0,6 = 48 мг (диоксид кремния + МКЦ + натрий кроскармеллоза);
- 80 мг / 0,712 × 0,210 = 24 мг (диоксид кремния);
- 48 мг – 24 мг = 24 мг (МКЦ + натрий кроскармеллоза).
Таблица 3. Результаты измерений

Адсорбция конго красного
Как тест-вещество для изучения адсорбции отрицательно заряженных низкомолекулярных соединений (натрия диклофенак, салицилаты, анальгин, аспаркам, соли жирных и желчных кислот и т. п.) применяют анионный азокраситель конго красный (М.м. = 697 г/моль).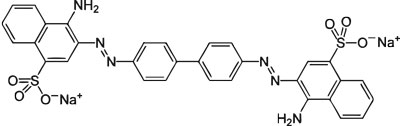
Рис. 7. Конго красный
Методика испытанияИсследуемый раствор. К 0,08 г (точная навеска) препарата добавляют 10 мл 0,7 мг/мл раствора конго красного, встряхивают на аппарате для встряхивания в течение 1 часа, потом центрифугируют при частоте вращения 6000 оборотов в минуту на протяжении 20 минут. 0,8 мл надосадочной жидкости доводят водой до 50 мл.Раствор сравнения. 0,8 мл 0,7 мг/мл раствора конго красного доводят водой до 50 мл.Измеряют оптическую плотность исследуемого раствора и раствора сравнения при длине волны 490 нм в кювете толщиной 1 см. В качестве компенсационного раствора используют воду.Адсорбционную активность препарата (Х, мг/г) рассчитывают по формуле, аналогичной как в случае измерений с метиленовым синим, где m – масса конго красного в 1 мл (0,7 мг).Результаты измерений отображены в Табл. 4.Таблица 4. Результаты измерений
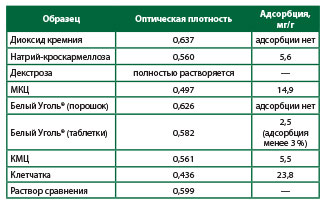
Адсорбция ионов цинка
Цинк выбран в качестве тест-вещества, которое моделирует отравление тяжелыми металлами: медью, свинцом, кадмием, ртутью, хромом и т. п. Концентрацию ионов цинка в растворе определяли экстракционно-фотометрическим методом с помощью дитизона.Дитизон — это специфический реагент, который образует с ионами тяжелых металлов, в частности с ионами цинка, комплексные соединения: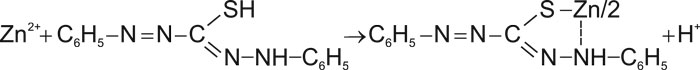
Рис. 8. Взаимодействие дитизона с ионами цинка
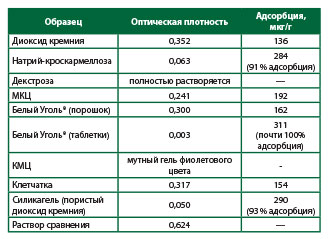
Методика испытанияГотовят раствор дитизона в СCl4 (10 мг дитизона в 400 мл растворителя).Исследуемый раствор. К 0,08 г (точная навеска) препарата добавляют 10 мл 2,5 мкг/мл раствора ионов Zn2+, встряхивают на аппарате для встряхивания 1 час, после чего центрифугируют при 6000 оборотов/мин на протяжении 20 минут. К 2 мл центрифугата добавляют 8 мл воды, 5 мл ацетатного буфера и 5 мл раствора дитизона. Смесь встряхивают в делительной воронке 2 минуты. После этого сливают нижний слой органической фазы в колбу. Снова добавляют 5 мл дитизона и повторяют экстракцию. Органические фазы объединяют.Раствор сравнения. К 2 мл 2,5 мкг/мл раствора ионов Zn2+ добавляют 8 мл воды, 5 мл ацетатного буфера и 5 мл раствора дитизона, далее выполняют двойное экстрагирование, как описано выше.Сразу после повторного экстрагирования измеряют оптическую плотность исследуемого раствора и раствора сравнения при длине волны 540 нм в кювете толщиной 1 см. В качестве компенсационного раствора используют холостую пробу, где на анализ берут 10 мл дистиллированной воды.Адсорбционную активность препарата (Х, мг/г) рассчитывают по формуле, аналогичной как для измерений с метиленовым синим, где m – масса цинка в 1 мл раствора (2,5 мкг).Результаты измерений отображены в Табл. 5.Таблица 5. Результаты измерений
Адсорбция белка (желатиновый тест)
В качестве тест-вещества, которое моделирует адсорбцию токсинов и метаболитов белковой природы с нерегулярным строением, используют желатин — продукт гидролиза коллагена.Методика испытания
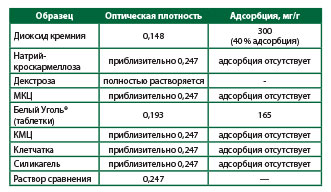
Исследуемый раствор. К 0,08 г (точная навеска) препарата добавляют 10 мл 6 мг/мл раствора желатина, встряхивают на аппарате для встряхивания в течение 1 часа, затем центрифугируют при частоте 6000 оборотов/мин на протяжении 20 минут. К 1 мл центрифугата добавляют 4 мл биуретового реактива, выдерживают 30 минут.Раствор сравнения. К 1 мл 6 мг/мл раствора желатина добавляют 4 мл биуретового реактива, выдерживают 30 минут.Измеряют оптическую плотность исследуемого раст-вора и раствора сравнения при длине волны 540 нм в кювете толщиной 1 см. В качестве компенсационного раст-вора используют холостую пробу (к 1 мл воды добавляют 4 мл биуретового реактива).Адсорбционную активность препарата (Х мг/г) рассчитывают по формуле, аналогичной для измерений с метиленовым синим, где m – масса желатина в 1 мл (6 мг).Результаты измерений приведены в Табл. 6.Таблица 6. Результаты измерений
Выводы
Измельченные таблетки Белый Уголь® (производитель ООО «ОМНИФАРМА КИЕВ», Украина) проявляют значительную адсорбционную активность в отношении метиленового синего и ионов цинка, почти полностью поглощая их из раствора. Но препарат в форме порошка, а также основные ингредиенты таблеток — диоксид кремнияи микрокристаллическая целлюлоза, каждый по отдельности, сорбируют эти вещества намного хуже.Таблетки Белый Уголь® имеют сбалансированный состав, где каждый ингредиент отвечает за адсорбцию определенного класса соединений и, следовательно, их комбинация придает препарату в целом широкие адсорбционные свойства. Таким образом, диоксид кремния характеризуется специфически высокой адсорбцией белка, натрий-кроскармеллоза — метиленового синего и ионов цинка, микрокристаллическая целлюлоза — конго красного.Адсорбция белка, основного фактора пищевой интоксикации, таблетками Белый Уголь® по сравнению с диоксидом кремния немного уменьшена (эффект «разбавления» неактивными в отношении белка ингредиентами), хотя остается достаточно высокой для проявления терапевтического действия.Таблетки Белый Уголь®, благодаря высокой адсорбционной активности, могут применяться не только в оздоровительно-профилактических, но и в лечебных целях.Одинаково эффективно сорбирует избранные тест-вещества клетчатка, которая является суммой нерастворимых и малорастворимых в воде соединений — целлюлозы, гемицеллюлозы, пектиновых веществ, лигнина и т. п. Карбоксиметилцеллюлоза, в состав которой входят отрицательно заряженные центры (ионизированные карбоксильные группы), согласно ожиданиям, лучше сорбирует катионный краситель метиленовый синий, чем конго красный (анион).![]() Литература
Литература
- Бойко А.М. Энтеросорбент/ Патент на полезную модель № 41849 (Украина), опубл. 10.06.2009, бюл. № 11. – 4 с.
- Геращенко И.И. Энтеросорбенты: лекарственные средства и диетические добавки. – К.: Ин-т химии поверхности НАН Украины, 2014. – 248 с.
- Доклиническое изучение энтеросорбентов. Метод. рекомендации / В.Г. Николаев, Н.Т. Картель, Е.А. Посохова и др. – Киев: Гос. эксперт. центр МЗ Украины, 2010. – 56 с.
- Геращенко И.И., Луценко В.А. Особенности контроля качества медицинских сорбентов // Фармац. журн. – 2010. –№ 5. – C. 37–41.
- Лурье Ю.Ю. Аналитическая химия промышленных сточных вод. – М.:Химия , 1984. – 448 с.
- Коренман И.М. Фотометрический анализ. Методы определения органических соединений. – М.: Химия, 1970. – 344 с.
- European Pharmacopoeia, 6-th Edition, 2007.






